Dieser Beitrag erscheint in der Reihe science&policy. In diesem Schwerpunkt setzt sich alexandria mit der Frage auseinander, wie Politik und Wissenschaft sich gegenseitig beeinflussen und wie die Wissenschaft bei gesellschaftspolitischen Entscheidungen helfen kann.
Mehr dazu findest du hier.
In Westdeutschland der späten Fünfziger ging die Angst um: Im ganzen Land häuften sich Berichte über Kinder, die mit verkürzten oder deformierten Gliedmaßen geboren wurden und oft die Geburt nicht überlebten. Die Verunsicherung war groß, das Leid der Betroffenen ebenso, doch was konnte die Fehlbildungen ausgelöst haben? Falsche Ernährung der Mütter, genetische Mutationen, radioaktive Strahlung? In Bayreuth stellte sich Karl Beck genau diese Frage. Der Kinderarzt schien 1958 eine Verbindung zwischen Fehlbildungen bei Embryonen und den Atomtests aufzuzeigen, die vor allem die USA und UdSSR seit Ende des Zweiten Weltkriegs durchführten. Diese Nachricht verbreitete sich in der Bevölkerung, die bereits von Berichten über die schädliche Strahlung sensibilisiert worden war. Beck schien zu bestätigen, was viele Bürger:innen dachten: „Immer wenn Atombomben explodieren, wurden kurz darauf im Bereich der fränkischen Klinik Embryos geschädigt, um sieben bis acht Monate später als missgebildete Kinder geboren zu werden.“ (Thomann, 2007)
Fehlalarm?
Auf Becks Alarm hin wurde auch die Bundesrepublik Deutschland tätig. Der Bundestag gab noch 1958 eine Erhebung in Auftrag, die klären sollte, ob seit 1950 mehr Fehlbildungen oder Totgeburten auftraten und ob ein Zusammenhang mit radioaktiver Strahlung bestand. Angesichts der fehlenden Strukturen und Daten in der jungen BRD eine organisatorische Herkulesaufgabe, die die Zusammenarbeit von Kliniken, Ärzteverbänden und Landesregierungen erforderte – ein bundesweites Gesundheitsministerium gab es noch nicht. Trotz der Schwierigkeiten entstand ein sorgfältiger und ausführlicher Bericht, der jedoch keinen Anstieg der Fehlbildungen seit 1950 feststellen konnte. Die Politik gab daraufhin Entwarnung, die Bevölkerung war beruhigt. Becks Vermutungen schienen sich als Panikmache herauszustellen, geschädigte Neugeborene waren nichts als traurige Einzelfälle. Nur manche Wissenschaftler:innen konnte der Bundestagsbericht nicht überzeugen. Sie ließen das Thema Fehlbildungen an Embryonen nicht gänzlich zur Ruhe kommen, auch nachdem die Politik die Akte schloss.
Erfolgsgeschichte Contergan
Schauplatzwechsel: In der rheinischen Stadt Stolberg stellten im Jahr 1954 Wilhelm Kunz und Herbert Keller zum ersten Mal Thalidomid her. Die Wissenschaftler forschten eigentlich für ihren Arbeitgeber Grünenthal zur Glutaminsäure, doch bald war klar, dass die Zufallsentwicklung Thalidomid eine bedeutende Errungenschaft war. Die Forscher stellten fest, dass Thalidomid eine beruhigende Wirkung besitzt. Außerdem zeigten sie, dass Thalidomid keine letale Dosis hat. Das war ein großer Vorteil gegenüber anderer damals üblicher Beruhigungsmittel. Gravierende Nebenwirkungen fanden die Wissenschaftler keine.
.png)
Abbildung 1: Das Medikament Contergan wurde schwangeren Frauen als Beruhigungsmittel verschrieben - mit schwerwiegenden Folgen.
Grünenthal setzte daraufhin Thalidomid im Medikament Contergan ein, das 1957 rezeptfrei auf den deutschen Markt kam. 1958 folgte auch in Österreich die Zulassung von Thalidomid unter dem Namen Softenon. Allerdings war Softenon dank dem Veto der Pharmakologin Ingeborg Eichler in Österreich rezeptpflichtig. Sie hatte als Mitglied der österreichischen Zulassungskommission eigene Tierversuche mit Thalidomid durchgeführt und aufgrund ihrer Ergebnisse gegen den rezeptfreien Verkauf in Österreich protestiert. Trotzdem wurde Contergan zum beliebtesten Schlaf- und Beruhigungsmittel Westdeutschlands. Immer mehr Ärzt:innen empfahlen das Mittel jedoch auch schwangeren Frauen, die an Morgenübelkeit litten.
Contergan war auch ein wirtschaftlicher Erfolg für Grünenthal. Über 300 Millionen Tabletten wurden in 47 Ländern verkauft, allein in Deutschland nahmen 5 Millionen Menschen Contergan. Der ausgezeichnete Ruf des Medikaments erhielt bereits 1959 erste Kratzer: Ärzt:innen berichteten über geschädigte Nerven bei Patienten, die mit Contergan behandelt wurden. Die Betroffenen litten an tauben oder kribbelnden Händen und Füßen. Grünenthal nahm daraufhin diese Nebenwirkung in die Packungsbeilage auf, um Contergan weiterhin rezeptfrei verkaufen zu können. Ohne Erfolg: Mitte 1961 wurde Contergan schließlich auch in Westdeutschland rezeptpflichtig.
Die Contergan-Katastrophe
1961, Contergan war drei Jahre am Markt, behandelte der Hamburger Kinderarzt Widukind Lenz 20 Kinder mit schweren Fehlbildungen. Angesichts dieser Schicksale begann er selbst Nachforschungen anzustellen. Lenz durchforstete Hausapotheken, befragte Ärzt:innen und Eltern. Im November 1961 präsentierte er einer Kinderärztetagung seine Vermutung: Contergan war für die Fehlbildungen verantwortlich. Waren zuvor unzählige frühere Warnungen ungehört geblieben, brachte der von Lenz aufgedeckte Contergan-Skandal den Hersteller Grünenthal dazu, Contergan am 27. November 1961 vom Markt zu nehmen – beinahe zwei Wochen, nachdem Lenz das Unternehmen informiert hatte. Die Contergan-Katastrophe konnte diese späte Erkenntnis nicht mehr verhindern.
Wurden 1958 in Deutschland noch etwa 24 geschädigte Kinder geboren, waren es 1961 bereits 1.515. Insgesamt wurden weltweit ungefähr 10.000 Thalidomid-geschädigte Kinder geboren, etwa die Hälfte überlebte die Geburt nicht. Es wird eine hohe Dunkelziffer vermutet. Je nachdem, in welcher Schwangerschaftswoche die Mütter Thalidomid eingenommen hatten, litten und leiden die Betroffenen an verkürzten oder fehlenden Gliedmaßen, an Fehlbildungen an Händen und Füßen, der Hüfte und des Verdauungstraktes, der Genitalien und Ohrmuscheln. Die eingenommene Dosis spielt für den Grad der Fehlbildungen keine Rolle.
Heute leben in Deutschland noch etwa 2.400 „Contergan-Kinder“. Da das Thalidomid-hältige Softenon in Österreich rezeptpflichtig war, leben dort offiziell nur noch ca. 20 Contergan-Opfer. Die Kinder von damals sind heute etwa 60 Jahre alt und leben mit den Spätfolgen der Contergan-Katastrophe: Sie leiden durch die jahrzehntelange Kompensation für fehlende oder fehlgebildete Gliedmaßen an schweren Erkrankungen des Bewegungsapparats und haben ein erhöhtes Schlaganfall- und Herzinfarktrisiko. Hinzu kommt eine starke psychische Belastung.
Die Contergan-Katastrophe hat unfassbares Leid verursacht. Doch wieso löst Contergan Fehlbildungen aus? Und wieso wurde das weder vor der Markteinführung noch in den über drei Jahren, in denen es verkauft wurde, erkannt?
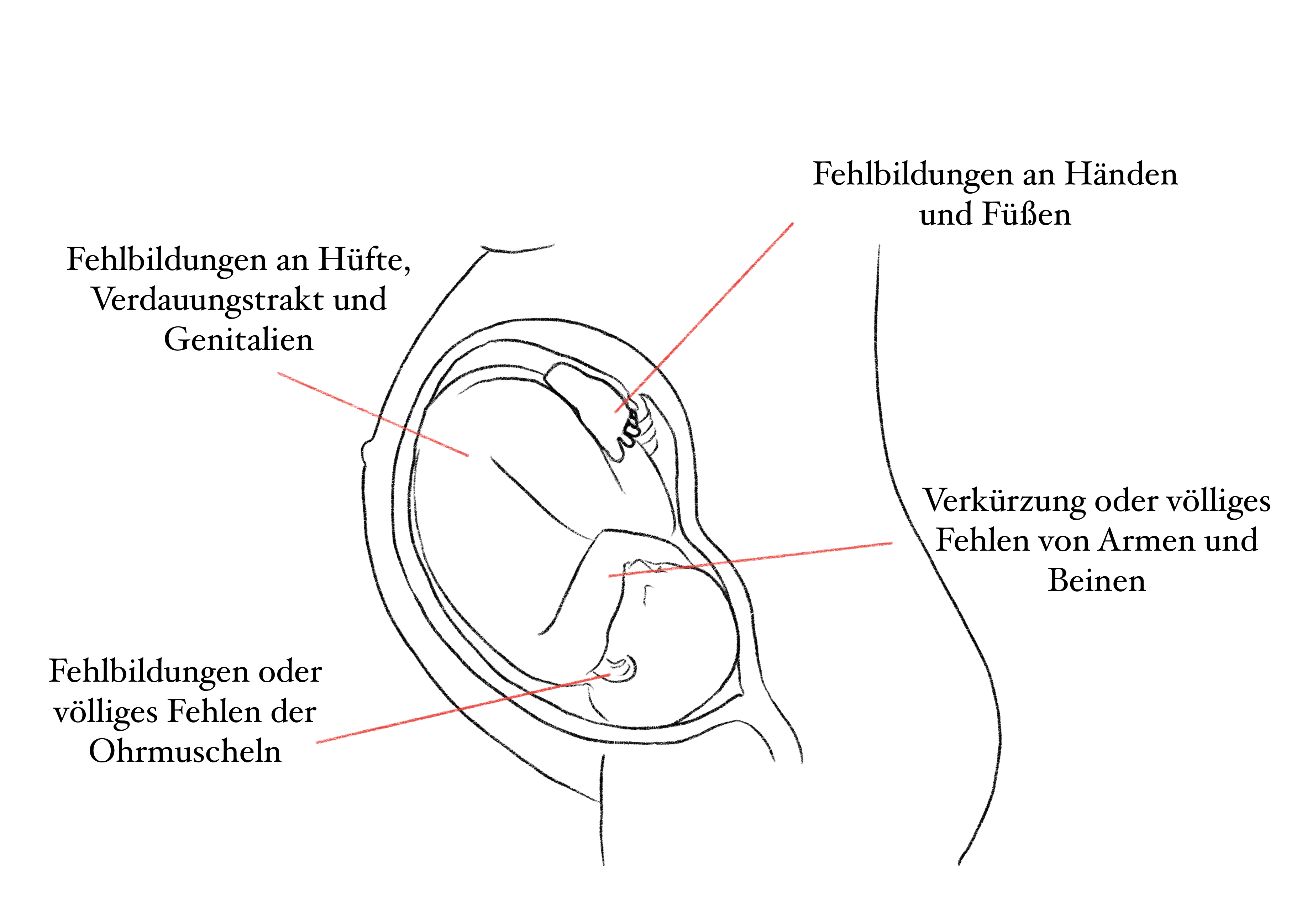
Abbildung 2: Der Inhaltsstoff Thalidomid konnte zu schweren Schädigungen bei dem neugeborenen Kind führen, je nachdem, ab welchem Zeitpunkt der Schwangerschaft die Mutter das Medikament einnahm.
C₁₃H₁₀N₂O₄
Der Wirkstoff von Contergan, Thalidomid, ist fruchtschädigend. Doch was ist Thalidomid überhaupt, und was passiert im Körper, wenn man es einnimmt? Thalidomid ist ein chirales Molekül mit der Summenformel C₁₃H₁₀N₂O₄. Moleküle werden als chiral bezeichnet, wenn sie in zwei Ausführungen vorkommen, die sich nicht durch eine Drehung ineinander überführen lassen. Die beiden Versionen, Enantiomere genannt, verhalten sich wie die linke und rechte Hand. Nur ein Enantiomer von Thalidomid ist teratogen, löst also Fehlbildungen bei menschlichen Embryonen aus. In Contergan waren beide Enantiomere enthalten. Doch selbst wenn man nur die vermeintlich harmlose Version zu sich nimmt, wandelt sie sich im Körper in ihr fruchtschädigendes Spiegelbild um.
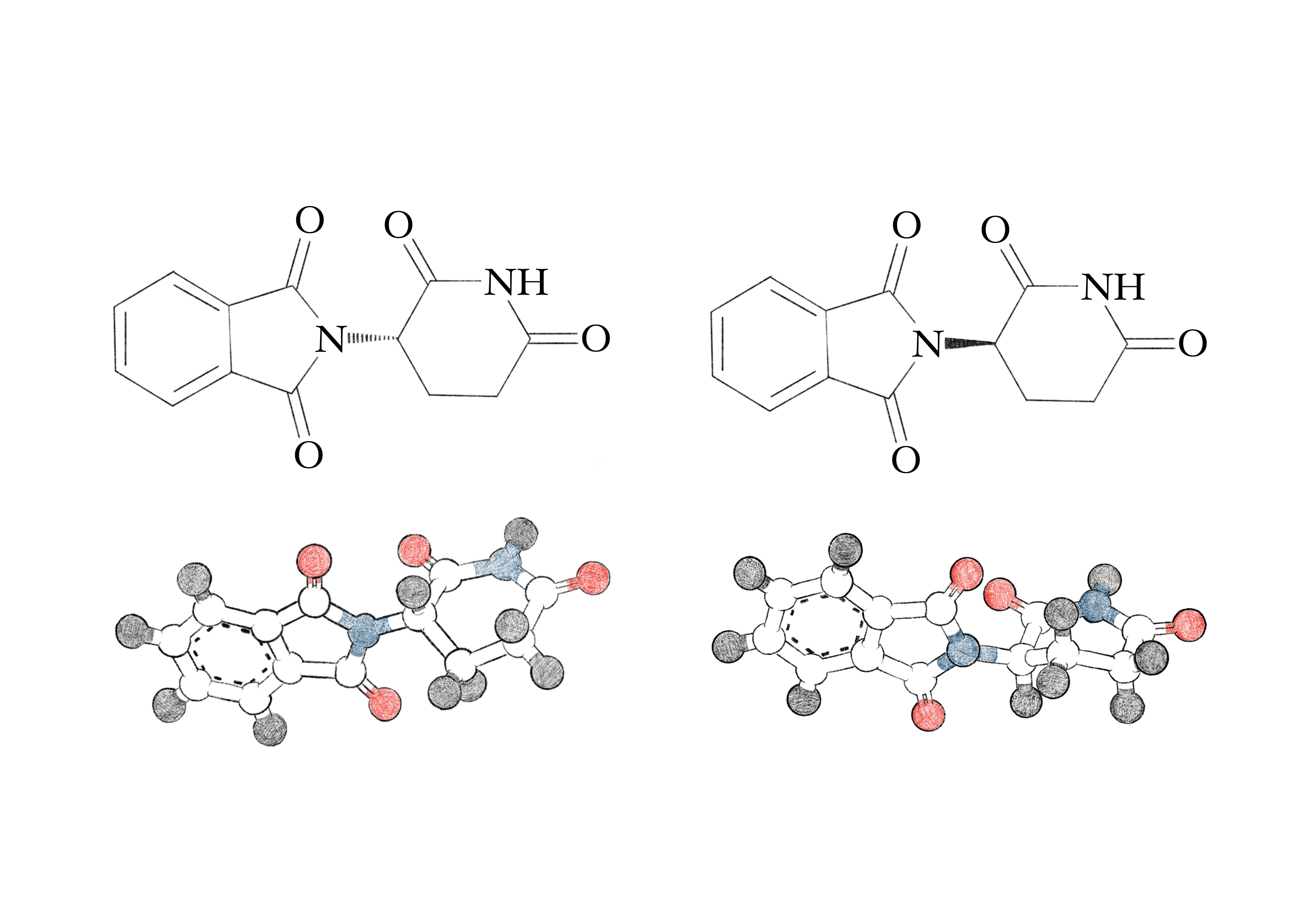
Abbildung 3: Die beiden Enantiomere von Thalidomid
Im Körper hemmt Thalidomid die Reizweiterleitung in den Nerven, indem es einen körpereigenen Botenstoff ersetzt. Dadurch entsteht der erwünschte Beruhigungseffekt. Wird Thalidomid während der Schwangerschaft eingenommen, so gelangt es auch in den Organismus des Embryos. Dort kann es an das Protein Cereblon binden, das in allen menschlichen Zellen vorkommt. Proteine sind Moleküle, die nach dem Schlüssel-Schloss-Prinzip funktionieren: Ihre Form erlaubt es, mit anderen Proteinen zu interagieren und so Prozesse im Körper einzuleiten, zu steuern oder zu hemmen. Dafür müssen aber die passenden Proteine zusammenkommen. Cereblon etwa bindet an Proteine und signalisiert damit, dass diese abgebaut werden müssen.
Kommt Thalidomid in Kontakt mit Cereblon, entsteht eine neue Struktur, die nun erlaubt, dass Cereblon an Proteine docken kann, die vorher nicht kompatibel waren. In den embryonalen Zellen befinden sich die Proteine Sall 4 und p63. Normalerweise steuern sie die Transkription der embryonalen DNA, die für Wachstum und Entwicklung der Gliedmaßen zuständig ist. Normalerweise würden auch Cereblon und Sall 4 sowie p63 nicht zusammenpassen. Doch das durch Thalidomid veränderte Cereblon bindet an die beiden Proteine, die in Folge abgebaut werden – der Embryo kann seine Gliedmaßen nicht oder nur eingeschränkt entwickeln.
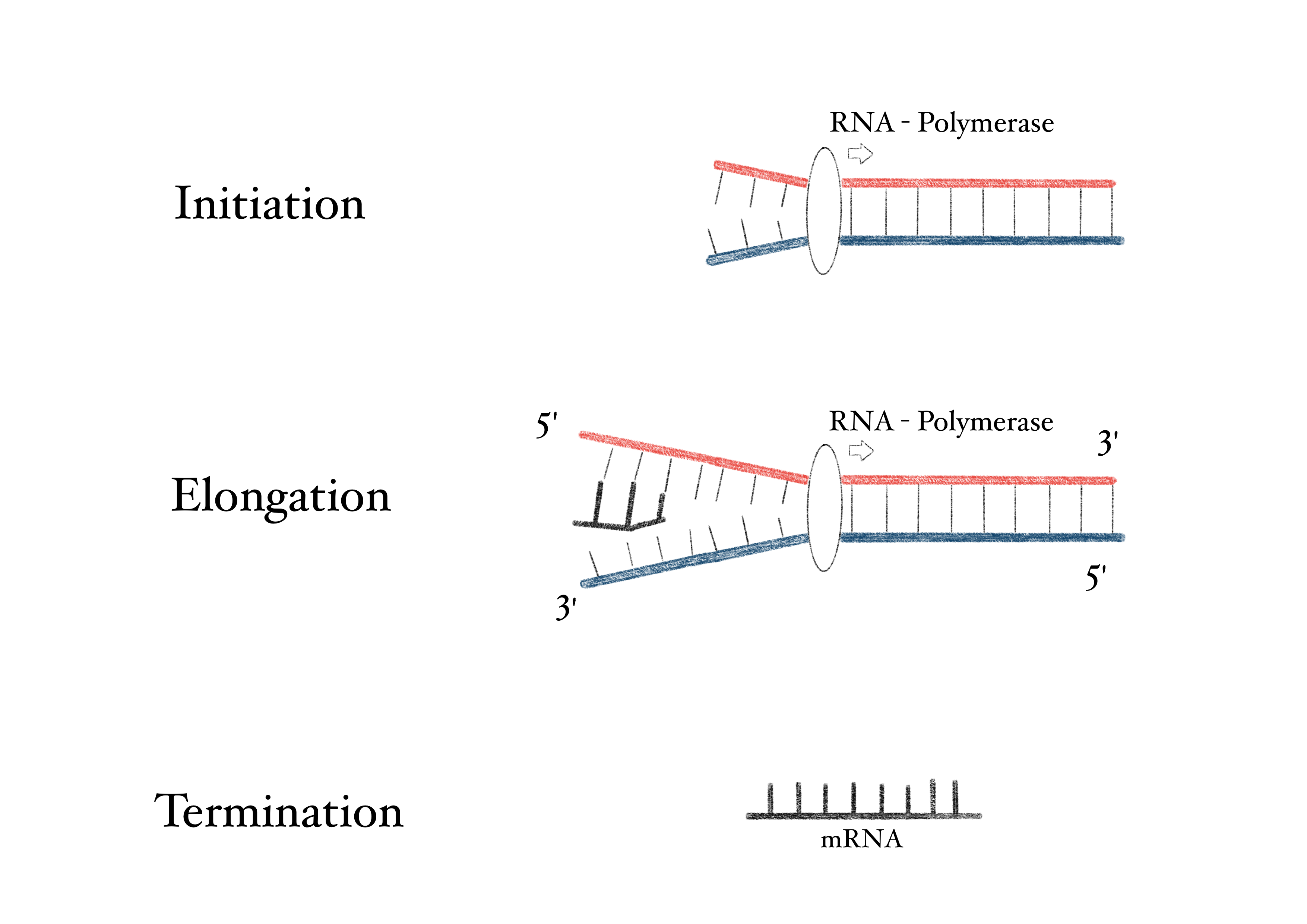
Abbildung 4: Der Transkriptionsprozess, in dem Cereblon an Proteine dockt und so Entwicklungsstörungen hervorrufen kann
Daten können täuschen
Was die moderne Forschung geklärt hat, war in den Fünfzigern unbekannt. Die damaligen Vorschriften zur Sicherheit von Arzneimitteln sahen nicht vor, dass Medikamente vor der Markteinführung auf teratogene Wirkungen getestet werden. Freilich wurden schon damals Tierversuche durchgeführt, die aber keine Hinweise auf Fehlbildungen zeigten. Das liegt daran, dass Thalidomid artspezifisch wirkt: Außer beim Menschen wurden nur noch bei einer Kaninchenrasse Fehlbildungen beobachtet. Daher war die teratogene Wirkung von Thalidomid besonders schwer zu entdecken.
Die ersten Thalidomid-geschädigten Kinder kamen bereits 1958 auf die Welt, ein Umstand, der durchaus bemerkt wurde. Nur wurde von Seiten der Medizin die Fehlbildungen beispielsweise als Folgen der Atomtests interpretiert. Als schließlich die von Karl Becks Vermutungen ins Rollen gebrachte Erhebung keinerlei Anstieg der Totgeburten und Fehlbildungen in Westdeutschland feststellen konnte, wurden die bereits von Contergan ausgelösten Schäden als „Ausreißer“ aus der Statistik angesehen, die man getrost ignorieren konnte. Die Botschaft, dass alles gut sei, wurde dann über die Politik an die besorgte Bevölkerung getragen, die weiter zu Contergan griff. Was ist hier schiefgegangen?
Die Kommunikation zwischen Politik und Wissenschaft war gut: Nachdem Ärzt:innen 1958 von gehäuften Fehlbildungen berichtet haben, wurde im selben Jahr eine gründliche Erhebung in Auftrag gegeben, die nach dem Arzt und Historiker Klaus-Dieter Thomann hohen wissenschaftlichen Standards genügte. Die Politik reagierte also schnell und richtig. Da Atomtests seit 1945 stattfanden, wählte man als Beobachtungszeitraum die Zeit nach 1950 aus, was ausreichend gewesen wäre, um einen Effekt der Strahlung nachzuweisen. Der beleuchtete Zeitraum endete jedoch kurz bevor die Welle der Contergan-Fehlbildungen über Deutschland hereinbrach und führte dazu, dass ihre ersten Vorboten nicht ernst genommen wurden.
Der Contergan-Skandal wurde auch gerichtlich aufgearbeitet. Im Mai 1968 begann der Contergan-Prozess am Landgericht Aachen. Der Prozess, der sich über 283 Tage hinzog, hatte zu klären, ob damalige führende Mitarbeiter von Grünenthal durch ihr Handeln oder Nicht-Handeln für die Opfer von Thalidomid verantwortlich waren. Der Contergan-Prozess wurde schließlich im Dezember 1970 eingestellt. Bezüglich der Thalidomid-geschädigten Kinder ging das Gericht von einer geringen Schuld der Angeklagten aus, da unter anderem Contergan nicht explizit an Schwangere vermarktet wurde. Außerdem nannte das Gericht als Grund für die Verfahrenseinstellung den Vergleich, den Grünenthal im Frühjahr 1970 mit den betroffenen Familien schloss – Grünenthal zahlte 100 Millionen D-Mark an die Opfer. Zusammen mit weiteren 100 Mio. D-Mark der BRD bildete diese Zahlung den Grundstock der 1971 gegründeten bundesdeutschen Conterganstiftung.
60 Jahre später
Viele Contergan-geschädigten Menschen führen heute ein selbstständiges Leben, gehen arbeiten, haben selbst Familien gegründet. Obwohl bei einigen der Zorn auf Grünenthal tief sitzt, haben sie gelernt, mit den Folgen von Contergan umzugehen. Fehlen etwa die Arme, so lernten manche Kinder früh, ihre Füße beinahe genauso geschickt einzusetzen. Doch was als junger Mensch funktioniert, löst im Alter Probleme aus, etwa Haltungsschäden oder Arthrosen.
Betroffene bildeten früh Selbsthilfegruppen und fordern von der Politik fehlende Anerkennung ein. Viele erhalten zwar eine Rente aus der Conterganstiftung – genug, um die oft kostspieligen Therapien und Anpassungen (etwa von Haus und Auto) zu decken, ist das nicht. Während in Deutschland die Aufarbeitung der Contergan-Katastrophe bald nach ihrem Bekanntwerden begann, wurde für österreichische Opfer erst 2015 eine Rentenleistung eingeführt.
Die Contergan-Katastrophe wurde durch fehlende Normen in der Arzneimittelsicherheit möglich. Sie wurde drei Jahre lang verkannt, da etwa der Einfluss von Atomtests als Ursache einzelner Fehlbildungen vermutet wurden und Grünenthal sowie Politiker:innen auf einen Parlamentsbericht verweisen konnten, der keinen Anstieg der Fehlbildungen nachwies. Erst zu spät wurde klar: Eine kleine Tablette war der Auslöser. Als Reaktion wurde weltweit der Verbraucherschutz verbessert und Gesetze angepasst. Unsere heutigen Sicherheitsstandards bei Medikamenten entstanden, um solche Arzneimittelskandale zu verhindern.
Die Contergan-Katastrophe zeigt, dass der Forschung Fehler passieren können, deren Ursachen sie möglicherweise nicht gleich erkennt. Das liegt im Wesen der Wissenschaft, sie produziert keine letztgültigen Wahrheiten. Daher ist es immer schwer, wenn politische Entscheidungen aufgrund wissenschaftlicher Forschung getroffen werden müssen. Reagiert etwa die Politik auf vorläufige Daten und Schlussfolgerungen, so geht sie das Risiko einer Fehlentscheidung ein. Reagiert sie nicht, so handelt sie verantwortungslos. Mit diesem Dilemma sind wir in der Pandemie täglich konfrontiert. Verständlich erscheint so die sich ausbreitende Skepsis der Forschung gegenüber. Doch letztlich bleibt die Wissenschaft unsere beste Möglichkeit, Fehler zu finden, Probleme zu beheben und weitere Fehler zu vermeiden, selbst wenn manche Erkenntnisse revidiert werden müssen. So waren es Wissenschaftler:innen, die schließlich die Ursache der Contergan-Katastrophe aufgedeckt haben und in Zusammenarbeit mit Politiker:innen weiteres Leid verhindern konnten. Und so zeigen uns auch Wissenschaftler:innen heute, wie wir mit der Corona-Pandemie zurechtkommen können.
Thomann, Klaus-Dieter (2007). Die Contergan-Katastrophe: Die trügerische Sicherheit der harten Daten. Deutsches Ärzteblatt 41, 2778 – 2782. (2.7.2021)
Der Contergan Skandal in Österreich (Bizeps, zuletzt abgerufen am 02.07.2021)
Der Pharmaunternehmer Grünenthal über den Contergan-Skandal aus Sicht des Unternehmens und über die Frage der Verantwortung: Der "Contergan-Skandal" und unsere Verantwortung heute (Grünenthal, zuletzt abgerufen am 02.07.2021)
Berichterstattung über den Prozess und Schadenersatz: Prozess endet im Vergleich (ORF, zuletzt abgerufen am 06.07.2021)
Eintrag über Thalidomid im Chemie-Lexikon (chemie.de, zuletzt abgerufen am 07.07.2021)
Contergan-Infoportal (zuletzt abgerufen am 08.07.2021)

.jpg)